1. In-Process Control(IPC)的来源
IPC可查到的最早、权威来源是(资料-1:Q7 Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients,原料药的GMP指南)
该指南的第8章即“Production and In-Process Controls”,描述该概念的段落语句如下:
8.30 Written procedures should be established to monitor the progress and control the performance of processing steps that cause variability in the quality characteristics of intermediates and APIs. In-process controls and their acceptance criteria should be defined based on the information gained during the development stage or historical data.
8.30 应制定书面程序,以监控会导致中间体和原料药质量特性产生变异的工艺步骤的进展,并控制其性能。过程控制及其可接受标准应根据开发阶段获得的信息或历史数据来确定。
8.31 The acceptance criteria and type and extent of testing can depend on the nature of the intermediate or API being manufactured, the reaction or process step being conducted, and the degree to which the process introduces variability in the product’s quality. Less stringent in-process controls may be appropriate in early processing steps, whereas tighter controls may be appropriate for later processing steps (e.g., isolation and purification steps).
8.31 可接受标准以及测试的类型和程度可能取决于所生产的中间体或原料药的性质、所进行的反应或工艺步骤,以及该工艺在多大程度上会导致产品质量产生变异。在早期工艺步骤中,较宽松的过程控制可能是适当的,而在后期工艺步骤(例如,分离和纯化步骤)中,更严格的控制可能更为适宜。
指南在术语中也给出了IPC的明确定义:
In-Process Control (or Process Control) 过程中控制(或过程控制)
Checks performed during production in order to monitor and, if appropriate, to adjust the process and/or to ensure that the intermediate or API conforms to its specifications.
在生产过程中进行的检查,目的是监控过程,并在适当时调整过程,和/或确保中间体或原料药符合其规格标准。
在ICH Q7中,IPC的定义主要是指在工艺过程中对中间体或原料液进行的检测,并且具有可接受标准。虽然没有明说,但推测应该更多的是指对中间体和原料药的质量属性的检测。
在(资料-2:ICH Q11 Development and Manufacture of Drug Substances (Chemical Entities and BiotechnologicalBiological Entities) 原料药开发和生产(化学实体和生物技术生物实体药物)),也给出了IPC的清晰描述。在ICH Q11中,IPC是作为控制策略的一部分提出。
6. Control Strategy 控制策略
6.1 General Principles 一般原则
A control strategy is a planned set of controls, derived from current product and process understanding, that assures process performance and product quality (ICH Q10). Every drug substance manufacturing process, whether developed through a traditional or an enhanced approach (or some combination thereof), has an associated control strategy.
控制策略是一套有计划的控制措施,源于对当前产品和工艺的理解,用于确保工艺性能和产品质量(ICH Q10)。每种原料药的生产工艺,无论通过传统方法、改进方法(或两者的某种结合)开发,都有相应的控制策略。
A control strategy can include, but is not limited to, the following:
控制策略可包括但不限于以下内容:
Controls on material attributes (including raw materials, starting materials, intermediates, reagents, primary packaging materials for the drug substance, etc.); 对物料属性的控制(包括原料药的原材料、起始物料、中间体、试剂、内包装材料等);
Controls implicit in the design of the manufacturing process (e.g., sequence of purification steps [biotechnological/biological drug substances], or order of addition of reagents [chemical entities]); 生产工艺设计中固有的控制(例如,纯化步骤的顺序 [生物技术 / 生物原料药],或试剂的添加顺序 [化学实体]);
In-process controls (including in-process tests and process parameters); 过程控制(包括过程检验和工艺参数);
Controls on drug substance (e.g., release testing);对原料药的控制(例如,放行检验);
在ICH Q11的指南中,IPC即为其名称所指的定义,即过程中控制。包含两部分,即过程中检验(IPT)和工艺参数的控制。这个概念相对于ICH Q7有了扩展。
后续很多指导原则和技术报告都延续了ICH Q11中对IPC的定义。比如(资料-3:PDA TR60 Process validation A Lifecycle Approach 工艺验证:生命周期方法),其对IPC的定义如下:
In-Process Controls 过程中控制
In-Process Controls (IPCs) are inputs to the process and are checks performed during production to monitor and, if appropriate, to adjust the process, and/or to ensure that the intermediates or product conform to specifications or other defined quality criteria.
过程中控制(IPCs)是过程的输入,是在生产过程中执行的检查,目的是监控过程,必要时调整过程,和/或确保中间体或产品符合标准或其他规定的质量标准。
2. In-Process Test(IPT)的来源
所能查到的关于IPT的最早来源是在(资料-4:Q6A Specifications Test Procedures and Acceptance Criteria for New Drug Substances and New Drug Products Chemical Substances 质量标准:新原料药和新药制剂的检测方法和可接受标准:化学药物),其中描述到:
2.3 In-process Tests 过程检测
In-process tests, as presented in this guideline, are tests which may be performed during the manufacture of either the drug substance or drug product, rather than as part of the formal battery of tests which are conducted prior to release.
本指导原则中所述的“过程检测 ”是指在原料药或制剂生产过程中进行的检测,而不属于出厂前的正式批检验。
In-process tests which are only used for the purpose of adjusting process parameters within an operating range, e.g., hardness and friability of tablet cores which will be coated and individual tablet weights, are not included in the specification.
某些生产过程中的检测,仅仅是为了在某一操作范围内调节工艺参数,如包衣前片芯的硬度、脆碎度及片重,而质量标准中一般不包括这些检测项目。
Certain tests conducted during the manufacturing process, where the acceptance criterion is identical to or tighter than the release requirement, (e.g., pH of a solution) may be sufficient to satisfy specification requirements when the test is included in the specification. However, this approach should be validated to show that test results or product performance characteristics do not change from the in-process stage to finished product.
某些生产工艺中进行的检测项目,其可接受标准与放行标准要求一致或更严格(如溶液的 pH)。 当某个检测项目订入质量标准中时,可能能够充分满足质量标准的要求,但在这种情况下,应对该方法进行验证,以表明检测结果或产品性能特性从生产阶段到成品未发生改变。
最终的术语定义中,IPT定义为:
In-process tests: 过程检测
Tests which may be performed during the manufacture of either the drug substance or drug product, rather than as part of the formal battery of tests which are conducted prior to release.
在原料药或制剂的生产过程中进行的检测,而不是常规放行检测中的一部分。
ICH Q6A主要内容是描述原料液或制剂的质量标准,并且将IPT作为该指南的一个小章节加以介绍,不难猜测中指南是将IPT定义为对过程中中间体的质量属性的检测。这其实是与ICH Q11的定义有所呼应,即IPC包含IPT和工艺参数的控制。
3. In-Process Monitor(IPM)的来源
在现有法规指南的知识库中没有查到IPM的权威来源。不过一些资料中的确有讲IPM代替IPT来使用。总体来看,IPM更像是公司内部自己的定义,而非法规指南中明确有描述的定义。
在查找资料中,看到Pfizer对IPT和IPM的定义和描述更有逻辑,也更容易理解,这里推荐一下(资料-5:Control Strategy Approach for a Well-Characterized Vaccine Drug Product,2020):
在文献中,对QA/CQA的监测称为In-process Test(IPT),同时将IPT分为了IPT-C和IPT-M,分别定义如下:
In-Process Test for Control (IPT-C): IPT-C is used to control a QA/CQA to within a specified value so that it meets desired DS/DP quality. IPTC has an associated acceptance criterion (e.g., protein concentration).
过程中控制测试(IPT-C):IPT-C 用于将QA/CQA 控制在规定值范围内,以使其满足期望的 DS/DP 质量。IPT-C 有一个相关的验收标准(例如,蛋白质浓度)。
In-Process Test for Monitor (IPT-M): IPT-M is used to measure a QA/CQA (1) to ensure that it is consistent with respect to previous process history or (2) for forward processing. The monitoring tests may have action limits (e.g., in-process impurity).
过程中监控测试(IPT-M):IPT-M 用于测量QA/CQA,一是为了确保其与先前的过程历史保持一致,二是为了后续加工。监控测试可能有行动限值(例如,过程中的杂质)。
理解来看,IPT-C是一个有可接受标准的IPT检测,而IPT-M则可以有,也可以没有可接受标准的IPT检测。
而在本文献中,Pfizer还同时规定了工艺参数的控制(control)和监控(Monitor),这也ICH Q11和ICH Q6中关于IPC和IPT的定义保持了一致。
总结来看,星辰对这三个定义的理解如下:
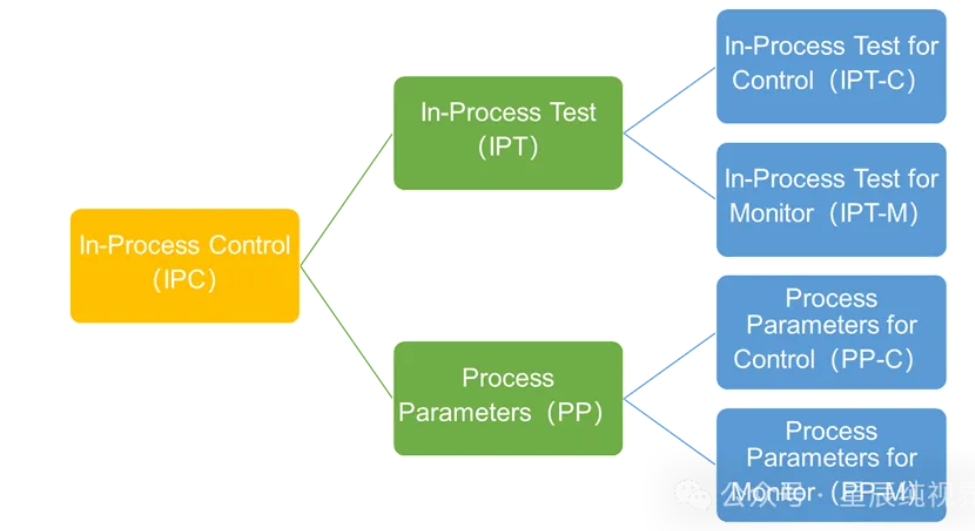
其实在工艺执行过程中,我们更应关注的是控制策略,而IPC是一个控制策略相关的术语概念,即指在工艺过程中所执行的控制。理论和实践上,这个过程中控制应当包含对过程中输入参数和输出属性的控制。
IPC中对输出属性的控制,称之为IPT,而对输入参数的控制并没有给出特定的定义,我们不妨简单称之为PP。无论IPT还是PP,根据其控制的严格程度,可以大致分为需要控制在标准内,以及只需要监控(不一定非要有标准)的控制,即上述的“control”和“Monitor”的区别。
这种理解方式和逻辑似乎要更清晰明白一些。在项目的不同阶段应该如何设定这些控制策略,将在下述的执行建议中给出星辰组织的理解和意见。
二:执行建议
控制策略设定的核心逻辑是:随着工艺知识和产品阶段的发展,从广泛的监控(Monitor)逐步聚焦和正式化为明确的控制(Control),并基于风险确定其严格程度。
1. 临床前与临床I/II期
广泛设置IPT-M点,收集大量数据(如多种代谢物、细胞状态多参数、多种杂质)。没有或仅有宽松的内部目标,目的是探索和建立初步的历史数据库。IPT-C则设定与安全性强相关的IPC,并带有行动限,比如微生物负荷和内毒素等。
此时还处于工艺开发阶段,工艺参数还在进一步的探索和优化,因此PP-C和PP-M都未有相关的设置。
2. 临床III期与工艺锁定
IPT-M可基于早期数据,将一部分IPM点取消(因信息价值低),另一部分转化为正式的IPT-C。与安全性强相关的IPC依然为IPT-C,并带有行动限(可能优化)。
工艺参数(PP),基于工艺表征的实验设计(DoE) 数据,识别的关键工艺参数 (CPP)从而建立PP-C和PP-M。
3. 商业化生产与生命周期管理
IPT和PP的所有内容将成为持续工艺确认(CPV)计划的关键部分,需要在商业化生产中监测和定期回顾,用于监控工艺稳定性和识别潜在漂移。
IPT-C和PP-C应严格按照注册标准执行。任何超出接受限或行动限的情况均按偏差处理。
在生命周期管理中也可以动态调整IPT和PP,比如将性能稳定的IPT-C和PP-C降级为IPT-M和PP-M,或者反向执行(出现趋势或者偏差时)。也可以考虑优化和调整IPT-C和PP-C的可接受范围。
我思考过这个问题,个人看法如下:
中间过程控制(In-process control, IPC)
通常使用分析测试方法或功能测试进行测量,以确保所选制造操作令人满意地实现预期的产品质量。IPC应设置可接受标准,因此IPC能够起到实质性的“控制”作用。
中间过程检测(In-process tests, IPT)
IPT通常认为是为了加强对工艺的理解,积累工艺数据,而开展的检测,IPT通常是不设置可接受标准的。可以通过对多批次生产的IPT数据分析来判断工艺表现稳健性和/或中间体质量属性的变化趋势,从而为纠正这些趋势或持续改进提供依据。因此一般认为IPT并没有实质性的“控制”作用。
中间过程监控(In-process monitor, IPM)
测试或评估选定的属性和/或参数,以了解设计空间内的产品质量或工艺性能趋势和/或增强对属性正态分布的信心。监控频率会定期审查并根据趋势进行调整。中间过程监控程序可能包括评估数据趋势的限度。
IPM与IPT在很多情况下是等同的,但似乎IPM范围更广,因为IPM还包含了对工艺参数的监控。
IPC也可以认为是IPT的一部分,区别在于IPC设置了可接受标准,对工艺和质量的“控制”有重要贡献。
结论:
没有明确的定义来区分这些概念,但这并不影响这种最佳实践的科学性与合理性。
作为申办方,我们在采用这种实践时,应在文件中对其进行定义,明确其作用和目的,以便监管机构理解和审评。
这{{threadTextType}}正{{isAdminText}}
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因: